Продолжаю публикацию лекции по применению в нефрологии принципов консервативного лечения хронических заболеваний (предыдущие части: 1 часть по возможностям немедикаментозного лечения [1], 2 часть по отдельным аспектам минеральных и костных нарушений [2]), приуроченной к Всемирному дню почки. В этой части значительное внимание будет уделено медикаментозному лечению, и назначению лекарственных препаратов по правилам, которые позволяют избежать развития побочных реакций.

Принципы консервативного лечения, конечно же, не ограничиваются только темой диеты и спорта. Поэтому давайте перейдем к рассмотрению вопросов, посвященных лекарственной терапии.
Если позволяет клиническая ситуация, то следует вводить в схему лечения один препарат за 1 раз. Тем самым мы сводим к минимуму возможность развития побочных действий за счет комбинации препаратов. Кроме того, если вы назначаете один препарат за один раз, то в случае развития побочных реакций вы точно знаете, от какого препарата это побочное действие разовьется. Если начать прием сразу 2 или 3 препаратов одновременно, и проявится какая-то побочная реакция, то будет сложно понять, какой из препаратов её вызвал.
К сожалению, этому правилу не всегда следуют. И можно услышать либо от знакомых, либо их сторонних разговоров когда автобус стоит в пробке, что пациенту врач одномоментно добавил к схеме лечения сразу два лекарства от артериальной гипертензии, у пациента давление 90 на 60, он себя плохо чувствует, и не знает что делать. Ситуация, когда на назначенные нами препараты развиваются такие негативные реакции, чревата сразу несколькими последствиями. Во-первых, сама по себе побочная реакция может быть довольно серьезной, вплоть до развития острого почечного повреждения. Во-вторых, у больного не развивается приверженность к длительному лечению. А для нас длительная приверженность лечению очень важна, в том числе в отношении хронической болезни почек. Если при протеинурии пациент следует нашим назначениям 1 или 3 месяца, а потом по собственной инициативе прекращает принимать назначенные лекарства, то такое лечение, в принципе, лишено смысла. Почему? Потому что и для нефрологов, и вообще для врачей любых специальностей, имеющих дело с хроническими заболеваниями, важна длительная приверженность больного к лечению и длительное подавление тех патофизиологических механизмов, которые приводят к развитию протеинурии, к повышению давления или к чему-то иному, и в конечном итоге – к снижению клубочковой фильтрации.
Оптимально, если любые препараты назначаются с малых доз, с последующим постепенным увеличением дозы либо до адекватной терапевтической, либо до максимально толерантной.
Важно избегать смены лекарств без достаточных оснований. Как говорится – “от добра добра не ищут”. Если препарат у больного хорошо работает, то лучше на нем и остаться, и десять раз надо подумать, а стоит ли менять его на другой.
Важно разъяснять пациенту план лечения, какие могут быть побочные действия и объяснить больному, что сам пациент должен в своем лечении участвовать.

В связи с возможным побочным действием лекарств надо особое внимание надо уделять пожилым, поскольку у них есть целый ряд факторов, которые развитие побочных реакций на лекарственную терапию, к сожалению, потенциируют. И в первую очередь эти факторы связаны с физиологическим уменьшением массы действующих нефронов с возрастом. Вы знаете, что где-то после 40 лет за счет возрастного склерозирования нефронов уменьшается суммарная скорость клубочковой фильтрации примерно на 1 мл/мин в год. Это физиологические темпы снижения СКФ. Соответственно, у пожилых пациентов скорость клубочковой фильтрации изначально может быть более низкой, что важно учитывать при назначении многих препаратов. Ведь почки играют очень важную роль в выведении или метаболизме большого числа лекарств. В принципе, прежде чем назначать пожилым любое лекарство, надо взять креатинин, рассчитать скорость клубочковой фильтрации, и в зависимости от нее дозировать эти препараты. И обязательно, если позволяет клиническая ситуация, начинать с малых доз, поскольку у пациентов со сниженной СКФ и фармакокинетика может быть изменена за счет уменьшения почечной экскреции, и фармакодинамика может быть изменена за счет каких-то других особенностей.
У пожилых часто имеется несколько сопутствующих заболеваний, подчас не связанных с почечной патологией, которые делают этих людей более ранимыми к любым воздействиям, и более склонными, в том числе, к развитию побочных реакций. Если у пациента несколько сопутствующих заболеваний, то ему каждый врач назначает свое лечение. Соответственно, у такого пациента есть целый букет медикаментов. И в отсутствии клинического фармаколога, что, к сожалению, чаще всего в российской практике и происходит, вероятность развития побочных эффектов существенно повышена.
Кроме того, важно помнить, что вообще у людей, и у пожилых в частности, есть риск взаимодействия лекарственных средств, которые назначит врач, и тех пищевых добавок, либо тех лекарств безрецептурного отпуска, которые пациенты сами покупают и начинают пить по своей инициативе. И если говорить о лекарствах безрецептурного отпуска, в первую очередь, это относится к нестероидным противовоспалительным препаратам. И пациентам с ХБП в обязательном порядке надо говорить – перед началом приема любого препарата, который ему назначит любой специалист, а тем более когда пациент сам увидит в рекламе очередную чудо-таблетку и захочет ее принимать – перед этим обязательно надо проконсультироваться с нефрологом.
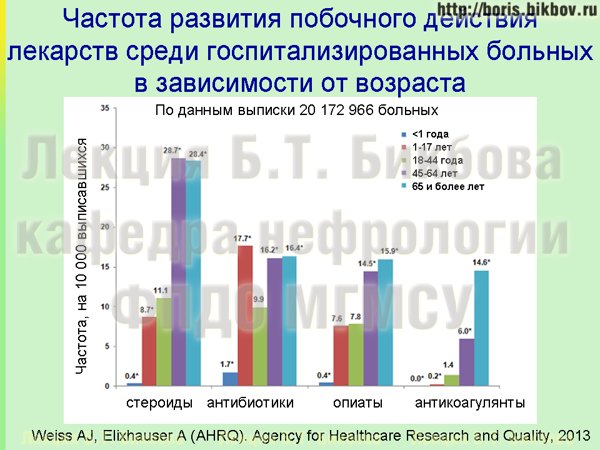
На этом слайде показана частота развития побочных реакций на лекарственные препараты по результатам 20 млн. госпитализаций – для четырех групп лекарств, которые чаще всего побочные эффекты вызывают. Наиболее часто фиксируются побочные реакции на фоне применения стероидов, антибиотиков, опиатов и антикоагулянтов. Это данные американские, у них опиаты более широко применяется для терапии болевого синдрома, у нас это конечно менее распространено. Но тем не менее, для остальных групп препаратов, а самое главное – для отдельных возрастных групп у нас закономерности остаются такими же. Синими столбцами показаны пожилые пациенты, и видно что у них намного чаще побочные реакции развиваются.
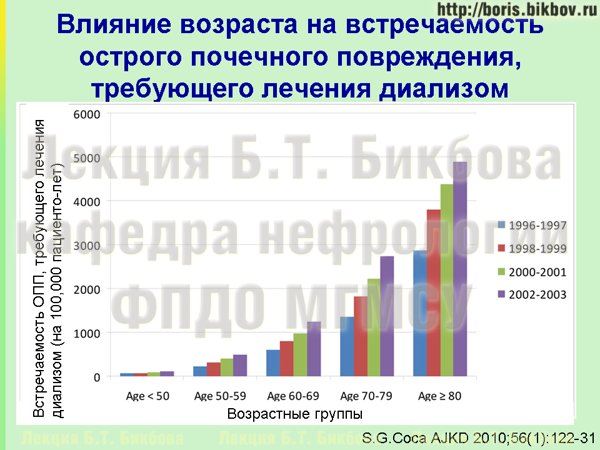
Если посмотреть на результаты другой работы, то они говорят о том, с какой частотой развивается острое почечное повреждение. И опять же видно, что пожилые пациенты, старше 60-70 лет, тем более – 80 лет, имеют намного более высокие риски развития острого почечного повреждения – как требующего лечения диализом, таки и не требующего лечения диализом. Вы знаете, что раз в году, во второй четверг марта, во всем мире отмечается Всемирный день почки. Каждый год для него выбирается определенная тематика, и закономерности, которые мы видим на слайде, объединяет тематику Всемирного дня почки в этом году (т.е. возрастные изменения почечной функции), и тематику Всемирного дня почки 2013 года (т.е. острое почечное повреждение [3]). Давайте более подробно об этой связи поговорим, перефразируя Ленина [4] – выдвинем основные мартовские тезисы.

Сам по себе термин “острое почечное повреждение” не всегда врачам и пациентам понятен, потому что он отличается от понятия “острая почечная недостаточность”. Термин “острая почечная недостаточность” обычно ассоциируется с выраженной тяжелой клиникой, массивными отеками, бледным отекшим пациентом, отеком легких и т.д. – все это указывает на очень выраженную дисфункцию почек. А концепция “острое почечное повреждение” (ОПП) позволяют раньше выявить негативное действие на почки, и клиника острого почечного повреждения может быть не так выражена, а биохимические изменения, рост креатинина крови, уже будет отмечаться. И нам важно помнить о тех группах пациентов, в которых острое почечное повреждение часто развивается, и проводить среди них активный скрининг на ОПП – чтобы максимально рано его выявить и не допустить дальнейшего развития, дальнейшего воздействия неблагоприятных факторов и ухудшения почечной функции.
Острое почечное повреждение очень распространено в общей популяции. По данным больших скрининговых исследований, которые проведены и в США, и в Европе, порядка 0,2-0,3 процентов всего населения за год переносят острое почечное повреждение. Это очень высокие показатели, которые означают что один из 300 или 500 человек в течение года имеют ту или иную степень ОПП. Среди госпитализированных пациентов в развитых странах, там, где эта статистика имеется, ОПП диагностируется почти у 15% пациентов. Что самое важное с точки зрения этих принципов консервативного лечения, о которых мы говорим, – это то, что каждого третьего или каждого пятого случая острого почечного повреждения можно избежать, и избежать в первую очередь за счет оптимизации лекарственного лечения, за счет назначения препаратов только тогда, когда они действительно нужны, и по схеме, которая минимизирует риск побочных реакций.
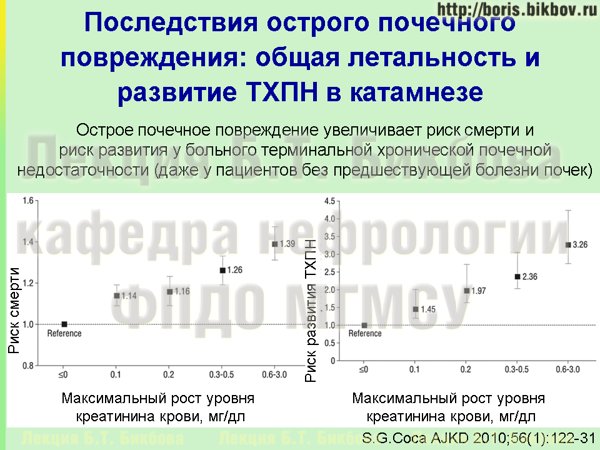
Каковы последствия острого почечного повреждения? Есть риск краткосрочный, который в ближайшие дни, недели и месяцы развивается, есть риск долгосрочный, который может проявляться на протяжении лет после эпизода ОПП. Краткосрочный риск – это повышение риска смерти у пациента с острым почечным повреждением. Причем вы видите, что это повышение имеется даже при незначительном росте креатинина в крови, и чем далее этот рост выше, тем выше риски и в краткосрочном, и в долгосрочном периоде. И даже с небольшого увеличения креатинина в крови при остром почечном повреждении у пациента отмечается и увеличение риска развития терминальной хронической почечной недостаточности в долгосрочной перспективе. Надо помнить, что почти половина случаев острого почечного повреждения остается недиагностированной, если специально не смотреть на уровень креатинина, поэтому крайне важно активно проводить скрининг на ОПП при приеме потенциально нефротоксичных препаратов.

Поэтому надо помнить о том, что есть группы препаратов, которые острое почечное повреждение наиболее часто вызывают (подробнее см. мини-лекцию по нефротоксичным препаратам [5]). Прежде всего, к ним относятся нестероидные противовоспалительные препараты. Они могут и при краткосрочном, и при длительном приеме приводить к поражению почек. Важно подчеркнуть, что все классы нестероидных противоспалительных препаратов, включая и селективные ингибиторы циклооксигеназы второго типа, и неселективные ингибиторы, обладают этим потенциальным нефротоксичным эффектом. Иногда можно прочитать в некоторых публикациях, что селективные ингибиторы не обладают нефротоксичностью, но, к сожалению, это не так.
Другой группой препаратов, которые могут приводить к побочным реакциям со стороны почек, являются антибиотики. В первую очередь, это относится к аминокликозидам, к амфотерицину В и к сульфаниламидам. При этом в большинстве ситуаций имеются альтернативы в отношении назначения этих антибиотиков, которые позволяют снизить риска нефротоксичности. А в ряде случаев применение нефротоксичных антибиотиков и вовсе не имеет преимуществ, например, это относится к комбинации цефалоспоринов с гентамицином при сепсисе [6]. В отношении амфотерицина В существуют хелированные формы, которые имеют риск нефротоксичности, но он почти в 2 раза ниже, чем у обычного амфотерицина.
Радиоконстрастные препараты, которые применяются при коронарографии, при других исследованиях с введением либо внутривенном, либо внутриартериальном контрастных препаратов, тоже могут давать ОПП. Соответственно, надо взвешенно подходить и к назначению диагностических исследований, и обязательно заниматься профилактикой развития контраст-индуцированной нефропатии.
Другие классы лекарственных препаратов, в частности, циклоспорин, такролимус, циклофосфамид, метотрексат, а также противоопухолевые препараты, литий, иноглобулины тоже обладают потенциальным нефротоксичным действием. К сожалению, в большинстве случаев их назначения нельзя избежать, мы их назначаем по совершенно определенным показателям, когда их применение жизненно необходимо.
Но вероятность развития нефротоксичности можно снизить. Во-первых, за счет того, что у пациентов, вынужденных применять какие-то из потенциально нефротоксичных препаратов, надо исключить сочетанный прием нескольких нефротоксичных лекарств. Причем надо активно опросить, не принимает ли больной какие-либо из этих препаратов, и обязательно сказать, чтобы на протяжении использования потенциально нефротоксичного препарата он не принимал других лекарства из этого списка. Во-вторых, нефротоксичность в значительной степени потенциируется гиповолемией. И, как правило, адекватная гидратация больного должна быть при приеме любых нефротоксичных препаратов. Есть ряд больных, у которых в обязательном порядке для профилактики острого почечного повреждения необходима внутривенная гидратация, вы это подробно разберете на отдельной лекции.

В рекомендации КДИГО по хронической болезни почек вошли ряд положений, которые соответствуют принципам консервативного лечения и нацелены на предотвращение развития нефротоксичных эффектов.
При хронической почечной недостаточности при назначении любого препарата важно учитывать СКФ и, при необходимости, менять дозировку или кратность приема в зависимости от СКФ. При серьезных интеркуррентных заболеваниях у больных со сниженной СКФ надо рассмотреть возможность, если это позволяет клиническая ситуация, временной отмены потенциальных нефротоксичных препаратов на период длительности этого серьезного интеркуррентного заболевания. На слайде эти препараты, над отменой которых следует подумать, перечислены – это НСПВП (нестероидные противовоспалительные препараты), метформин, препараты лития, дигоксин.
Я хочу обратить ваше внимание, что к потенциально нефротоксичным препаратам относится и ингибиторы ангиотензин-превращающего фермента, и блокаторы рецепторов ангиотензина, и ингибиторы ренина и блокаторы альдостерона – то есть все те лекарства, которые мы применяем для нефропротекции, для замедления снижения скорости клубочковой фильтрации и предотвращения прогрессирования почечной недостаточности. Но для большинства пациентов, при соблюдении всех необходимых мер, эти препараты никогда не проявят нефротоксичного эффекта. Для подавляющего большинства больных эти препараты позволяют замедлить прогрессирование почечных заболеваний.
Еще один класс лекарственных препаратов, который может потенциировать развитие нефротоксичных эффектов – это диуретики. Этот побочный эффект связан с тем, что диуретики могут приводить к развитию гиповолемии и изменению внутрипочечной гемодинамики. Важно в отношении диуретиков помнить, что назначая диуретик у стабильного пациента, мы преследуем цель не увеличения диуреза, а увеличение натрийуреза. Не знаю, насколько последняя фраза прозвучала понятно и насколько вы ей придаете значение, поэтому поясню ее чуть подробнее. Когда пациенту с ХБП, или вообще любому пациенту, назначается диуретик, то важно понимать для чего это делается. Если у пациента нет явных симптомов гиперволемии и задержки жидкости, то у него не требуется экстренная коррекция водного баланса в организме, поэтому мы диуретики даем не с целью увеличения количества мочи, а с целью увеличения экскреции натрия с мочой. И, соответственно, диуретики для натрийуреза даются в небольших дозах и в течение длительного периода времени. Тогда как диуретики с целью собственно диуреза – увеличения объема мочи – даются в относительно больших дозах на тот период времени, пока не ликвидируется явная гиперволемия.
Очень широко применяемым классом потенциально нефротоксичных препаратов являются нестероидные противовоспалительные лекарства, обезболивающие препараты. Доказано, что сочетание приема ИАПФ с нестероидными противовоспалительными препаратами, либо нестероидных препаратов с препаратами лития существенно увеличивает риск развития острого почечного повреждения, поэтому сочетаний этих надо избегать. В целом, следует вообще избегать одновременного приема нескольких потенциально нефротоксичных препаратов.

Пациентам с ХБП не рекомендуется использование растительных препаратов, это положение вошло в рекомендации КДИГО потому, что большинство растительных препаратов малоизучено, в том числе мало известно об их потенциальных нефротоксичных эффектах.
Пациент с ХБП должен проконсультироваться с врачом перед приемом любых лекарств, включая и пищевые добавки. Пациенту об этом обязательно надо говорить, как только он появляется в поле зрения нефролога. Больному надо и говорить, и давать памятку об этом (мы попозже об этом скажем) – что он должен и что он не должен делать. В частности, надо говорить: вы должны консультироваться с врачом при каких-то существенных интеркуррентных заболеваниях, если это касается больных со сниженной СКФ, и должны консультироваться с нефрологом перед приемом любых других лекарственных препаратов.
Метформин – это препарат первой очереди для монотерапии сахарного диабета 2 типа. Хотя сам метаформин не обладает нефротоксичным действием, однако надо помнить, что у него преимущественно почечная элиминация, и у больных со скоростью клубочковой фильтрации менее 45 мл/мин терапевтическое окно этого препарата уменьшается, соответственно – увеличивается риск серьезных осложнений. Поэтому в рекомендации КДИГО вошли положения по использованию метформина и других гипогликемических препаратов в зависимости от скорости клубочковой фильтрации у больного. При СКФ более 45 мл/мин прием метформина возможен, при СКФ 30-45 мл/мин надо очень осторожно и взвешенно к его назначению подходить, а при СКФ менее 30 мл/мин этот препарат рекомендуется отменить.
У пациентов, которые проходят короткий курс этих потенциально нефротоксичных препаратов, необходимо мониторировать маркеры развития острого почечного повреждения. А у больных, которые длительно применяют эти потенциально нефротоксичные препараты – надо периодически проводить скрининг на развитие ХБП – это анализ мочи и определение креатинина крови с расчетом СКФ.

Как я уже сказал, надо помнить о том, что даже нефропротективная терапия, которую мы назначаем с целью замедления прогрессирования болезней почек, – ИАПФ, БРА, прямые ингибиторы ренина и блокаторы рецепторов альдостерона – могут обладать потенциально нефротоксичным эффектом. Поэтому к их назначению надо подходить взвешенно, важно проводить мониторингу побочных реакций при их приеме. И это позволит обеспечить успех применения ИАПФ или БРА с минимизацией рисков побочных действий. Важно подчеркнуть, что у значительного большинства пациентов с хроническими нефропатиями применение ИАПФ и БРА является основным компонентом нефропротективного лечения, и преимущества их применения у большинства больных в виде замедления снижения СКФ существенно превосходят их возможные побочные эффекты.

Мы возвращаемся к принципам консервативного лечения хронических заболеваний. Они говорят о том, что надо быть внимательны к побочным действиям лекарств и помнить о том, что ряд препаратов могут давать ухудшение симптоматики со стороны разных органов. В частности, прием нестероидных противовоспалительных препаратов больными может приводить за счет подавления синтеза простогландинов в почках к задержке жидкости и, соответственно, к усугублению сердечной недостаточности. Причем если мы у больного активно не спрашиваем или не придаем значения тому, что он принимал нестероидные противовоспалительные препараты, то мы будем думать – нам надо усилить терапию сердечной недостаточности, увеличить дозу или добавить тот или иной класс препаратов. К сожалению, в таком случае за счет этой ошибочной тактики можно повысить риск развития побочных реакций, риск развития острого почечного повреждения. Поэтому, если у пациента есть те или иные симптомы, или появляются те или иные симптомы, то необходимо задуматься, могут ли быть они вызваны уже назначенной терапией, и тогда надо попытаться отменить эти препараты, которые могут такие симптомы вызвать, а не пытаться вышибить клин клином.
Конечно же, пациент должен быть информирован о возможных побочных действиях. Пациент также должен быть информирован о синдроме отмены – ведь довольно часто у пациента, который длительно принимает препарат, бывает желание бросить, просто прекратить лекарство пить. И пациент должен знать, что значительное число лекарственных препаратов нельзя прекращать сразу пить на следующий день, надо обязательно перед таким решением посоветоваться с врачом, и отменять большинство препаратов надо постепенно, либо необходимо один препарат заменять их на другой.

Следующим принципом консервативного лечения является взвешенный подход к стремлению к инновациям и к тому, что уже хорошо известно во врачебной практике. В арсенале врача регулярно появляются новые препараты, и обычно, к моменту начала их использования в мире имеется много информации об их положительных эффектах, собственно терапевтическом действии. В большинстве случаев к моменту начала использования в практике для лекарственных препаратов еще не накоплен достаточный опыт по побочным действиям препарата, в том числе и по потенциально нефротоксичным эффектам. Именно поэтому важен постмаркетинговый мониторинг применения лекарственных препаратов в реальной клинической практике – чтобы понять соотношение плюсов и минусов для конкретного медикамента. Важно помнить, что при назначении недавно появившихся на рынке препарата надо следовать разумному компромиссу между стремлением назначить новый, может быть более эффективный препарат, и теми побочными реакциями, которые еще могут быть недостаточно изучены. Следует думать об этом компромиссе, решая – назначить ли уже известное и достаточно давно имеющееся в практике лекарство, которое хорошо работает, и побочные эффекты которого известны, либо назначить новое лекарственное средство, может быть с не вполне изученным соотношением пользы и риска.
Важно использовать независимый источник информации о лекарственных препаратах. И в этом смысле важно уметь оценивать публикации в научной литературе, понимать насколько хорошо проведено исследование, насколько его результаты применимы к больному, который сидит у вас на приеме.
И, наконец, важно в этом разумном выборе назначения препаратов ориентироваться на клинически значимые исходы, а не на суррогатные показатели. Клинически значимые исходы – это летальность, это развитие осложнений, которые можно четко диагностировать (инфаркт миокарда, инсульт, и т.д.), в определенной мере – это качество жизни. А суррогатные показатели – это те лабораторные маркеры, которые мы определяем и о которых мы думаем, что они связаны с клинически значимыми исходами.

В отношении роли суррогатных и клинически значимых показателей достаточно демонстративна история с коррекцией анемии у больных на диализе. За последние несколько лет, точно так же как и в отношении коррекции вторичного гиперпаратиреоза у больных на диализе, несколько раз пересматривались концепции терапии. И в нынешнем варианте рекомендаций KDIGO, которые переведены на русский язык, постулируется важность разумного ограничения применения эритропоэз-стимулирующих препаратов, применения препаратов железа, сейчас изменены целевые значения уровня гемоглобина у больных на диализе.
Коррекция анемии у большинства больных рекомендуется только при снижении гемоглобина менее 100 грам на литр, а целевым уровнем считается гемоглобин не более 115 г/л. Если вы знакомы с предыдущими рекомендациями, то видно некоторое уменьшение целевого уровня гемоглобина. Это уменьшение произошло как раз вследствие приверженности тому принципу консервативного лечения, о котором мы сейчас говорим. Раньше целевые значения уровня гемоглобина принимались выше, в первую очередь, с учетом суррогатного показателя – уровня гемоглобина крови. Но в результате относительно недавно завершенного анализа рандомизированных контролируемых исследований по коррекции анемии, в которых прежде всего оценивали клинически значимые исходы (частоту инсультов, инфарктов, смертей), было показано, что избыточное применение препаратов для коррекции анемии, и достижение за счет них более высоких уровней гемоглобина может приводить к увеличению риска тромбозов, риска кардиоваскулярных осложнений. Конечно же, клинически значимые исходы для принятия решения в медицине намного важнее суррогатных показателей.

Важно ориентироваться не только на то, что мы думаем о препарате, о том, как он действует на биохимическом уровне, как он действует на те или иные органы или системы, а ориентироваться на результаты клинических исследований.
Одним из применений этого принципа является то, что в настоящее время в рутинной клинической практике для большинства пациентов не показано сочетание ИАПФ и блокаторов рецепторов ангиотензина, которое недавно довольно широко предлагалось. Это изменение произошло именно из-за того, что раньше в нефрологическом сообществе было представление, что хорошо эти препараты комбинировать с точки зрения патофизиологии, поскольку они действуют на разные звенья ренин-ангиотензин-альдостероновой системы. Но когда получили результаты клинических исследований, в которых анализировались клинически значимые исходы одновременного их приема, то оказалось, что комбинация ИАПФ и БРА у одного больного связана с повышением риска побочных эффектов. Сейчас проводятся другие клинические исследования, с другими схемами сочетанного назначения ИАПФ и БРА, или назначения такой комбинации в строго отобранных группах пациентов, с обязательным учетом всех эффектов – и благотворных, и негативных – такой терапии. И только после завершения этих исследований можно будет судить о возможности комбинированного лечения ИАПФ и БРА в клинике.
Важно помнить о том, что среди тех статей, которые публикуются в журналах, имеется положительная селекция – когда авторами доказан хороший результат или эффективность, когда имеются данные по превосходству одного лекарственного препарата по сравнению с другим, то эту статью заведомо более вероятно опубликуют, и сами авторы ее заведомо более вероятно напишут. Тогда как статьи, в которых любой препарат не показал эффективности, или воздействие двух лекарств было одинаковым, и авторы пишут менее охотно, и многие журналы их не так активно публикуют. Масштабы этой диспропорции между “положительными” и “нейтральными” статьями настолько велики, что сейчас учреждены специальные журналы, которые специализируются на публикации только таких “нейтральных” или “отрицательных” результатов, например, Journal of Negative Results in BioMedicine [7].
Наконец, важно ориентироваться не только на данные рандомизированных контролируемых исследований, хотя они и являются золотым стандартом для медицины, но и на результаты анализа эффективности, частоты побочных эффектов, и безопасности в реальной клинической практике – в постмаркетинговых исследованиях.

В принципах консервативного лечения целый набор положений говорит о необходимости вовлечения больного и в принятие решений, и, что самое главное, в собственное лечение. Как говорил кто-то из древних, когда к нему приходил больной: “Нас трое – я, ты и болезнь. И если ты будешь на стороне болезни, то победит она. Если ты будешь на стороне врача, то мы вместе победим болезнь”. Принципы консервативного лечения в несколько более формализованной форме о том же самом и говорят. А именно о том, что врачу следует стараться активизировать больного, чтобы пациент был на стороне врача и активно со своей болезнью боролся. Для этого важно информировать пациента о том, что хронические заболевания требуют хронического лечения. В течение болезни, на протяжении лет или десятилетий, надо принимать медикаменты постоянно, по совету врача можно менять дозировку, добавлять или убирать какие-то лекарства в зависимости от меняющейся симптоматики, но, тем не менее, базовым принципом у подавляющего числа больных является наличие некоего медикаментозного фона, наличие постоянного приема лекарств, которые эту хроническую болезнь корригируют. При этом, конечно, не надо забывать и о возможностях немедикаментозного лечения (диеты, физической активности, отказа от вредных привычек, и т.д. [1]), которых обычно бывает недостаточно для полной коррекции заболевания, но которые существенно помогают лекарственной терапии.

Важно осмысленно подходить и к просьбам пациента, и к предложениям представителей фармкомпаний назначить новый препарат. Кроме того, прежде чем назначить новый препарат или увеличить дозу уже выписанного, следует убедиться в том, что больной назначенные препараты принимает. По результатам отдельных исследований, в течение первого года лечения почти 20% больных артериальной гипертензией отказываются от приема антигипертензивной терапии. Понятно, что в такой ситуации, если больному выписать еще один препарат, это ничего не даст. Надо в первую очередь добиться того, чтобы пациент следовал тем назначениям, которые уже есть.
Наконец, в особенности, для коррекции артериальной гипертензии, важно варьировать дозу препаратов, уменьшать или увеличивать ее, в зависимости от степени подъема артериального давления. Такой подбор терапии под текущую клиническую картину, периодическое переосмысление тактики лечения больного, важен для того, чтобы, с одной стороны, избежать гипотензивных эпизодов, которые в том числе и на почки плохо воздействуют, а с другой стороны, чтобы избежать и недостаточного воздействия на те патофизиологечские звенья, которые приводят к повышению артериального давления.
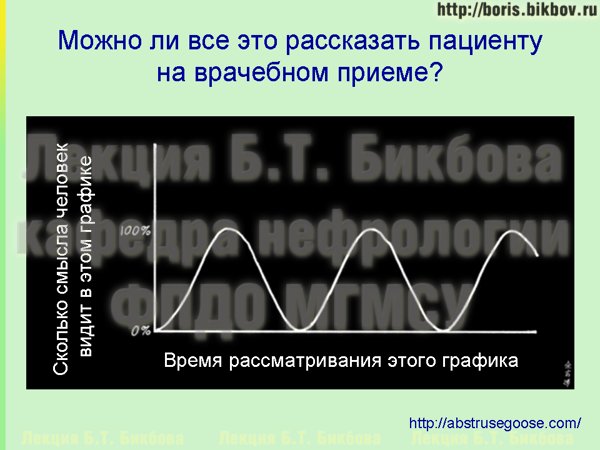
Посмотрите на этот шуточный график, нарисованный одним из квантовых физиков, и оцените его применимость к медицине. Здесь по вертикальной оси, от 0 до 100 процентов, отложено сколько смысла человек видит в этом графике, когда на него смотрит. А по горизонтали отмечено время, в течение которого этот график рассматривается. Соответственно, если говорить о врачебной практике, об амбулаторном приеме, то очевидно что прием длится совсем недолго, и у врача нет возможности подробно рассказать все эти принципы больному. Информация, которую получает больной во время консультации, обычно занимает на этом графике самое начало восходящей волны синусоиды. Кроме того, информацию и рекомендации, которые врач пациенту во время приема дает, в значительной степени может либо не запоминаться, либо не совсем правильно оцениваться пациентом, и это подтверждается результатами целого ряда исследований.

На приеме реально ответить только на текущие вопросы больного, но всю информацию о болезни “от А до Я” каждому пациенту рассказывать невозможно. Поэтому есть книги и брошюры для больных с заболеваниями почек на русском языке. Те книги и брошюры, о которых я знаю, можно найти на этой странице [8]. Значительную часть этих информационных материалов, практически все, можно бесплатно скачать, и можно пациенту этот список дать для того, чтобы он самостоятельно знакомился с этой литературой. Все эти книги и брошюры написана для пациентов таким языком, чтобы наиболее просто объяснить что такое хроническая болезнь почек, как надо проводить профилактику почечных заболеваний, как надо придерживаться немедикаментозной терапии, как надо принимать лекарства, и о других вещах, о которых пациент должен знать, в том числе и для того чтобы вместе с врачом бороться против своего заболевания.